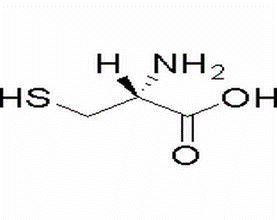
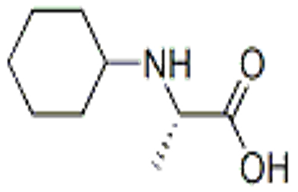L-cisteina (CAS# 52-90-4)
| Simboli di pericolo | Xn – Nocivo |
| Codici di rischio | R22 – Nocivo per ingestione R36/37/38 – Irritante per gli occhi, le vie respiratorie e la pelle. |
| Descrizione di sicurezza | S26 – In caso di contatto con gli occhi, lavare immediatamente e abbondantemente con acqua e consultare un medico. S37/39 – Usare guanti adatti e proteggersi gli occhi/la faccia |
Introduzione
La L-cisteina (L-cisteina) è un amminoacido non essenziale, codificato dai codoni UGU e UGC, ed è un amminoacido contenente solfidrile. A causa della presenza di gruppi sulfidrilici, la sua tossicità è ridotta e, come antiossidante, può prevenire la generazione di radicali liberi. & & La L-cisteina è un amminoacido non essenziale presente in natura. È un attivatore di NMDA. Svolge anche molti ruoli nella coltura cellulare, come segue: 1. Substrato per la sintesi proteica; Il gruppo sulfidrilico nella cisteina svolge un ruolo importante nella formazione dei legami disolfuro ed è anche responsabile del ripiegamento delle proteine e della generazione di strutture secondarie e terziarie. 2. Sintesi dell'acetil-CoA; 3. proteggere le cellule dallo stress ossidativo; 4. è la principale fonte di zolfo nelle colture cellulari; 5. Ionoforo metallico. & & Attività biologica: la cisteina è un α-amminoacido polare contenente gruppi sulfidrilici nel gruppo alifatico. La cisteina è un amminoacido essenziale condizionale e un amminoacido saccarogenico per il corpo umano. Può essere convertito dalla metionina (metionina, un amminoacido essenziale per il corpo umano) e può essere convertito in cistina. La decomposizione della cisteina viene decomposta in piruvato, idrogeno solforato e ammoniaca attraverso l'azione della desolforasi in condizioni anaerobiche, o attraverso la transaminazione, il prodotto intermedio β-mercaptopiruvato viene decomposto in piruvato e zolfo. In condizioni di ossidazione, dopo essere stato ossidato in acido solforoso cisteina, può essere decomposto in piruvato e acido solforoso mediante transaminazione e decomposto in taurina e taurina mediante decarbossilazione. Inoltre, la cisteina è un composto instabile, facilmente redox e interconverte con la cistina. Può anche essere condensato con composti aromatici tossici per sintetizzare l'acido mercapturico per disintossicarsi. La cisteina è un agente riducente, in grado di favorire la formazione del glutine, ridurre il tempo necessario per la miscelazione e l'energia necessaria per l'uso medicinale. La cisteina indebolisce la struttura della proteina modificando i legami disolfuro tra le molecole proteiche e all'interno delle molecole proteiche, in modo che la proteina si distenda.